Derivación linfática microquirúrgica múltiple en el tratamiento de la quiloascitis masiva - Multiple Lymphvenous Anastomosis for Massive Chylous Ascites
Keywords:
ascitis, ascitis quilosa, microcirugía, anastomosis linfático-venosa, ascites, chylous ascites, microsurgery, lymphvenous anastomosisAbstract
ResumenLa quiloascitis es la acumulación excesiva de linfa en la cavidad abdominal con respecto a la producción normal, lo que tiene múltiples consecuencias. Su etiología es diversa, siendo el trauma la principal causa, y en este grupo se encuentran las quiloascitis secundarias a diferentes procedimientos quirúrgicos intraabdominales, en especial los que implican la manipulación del retroperitoneo. Cuando se presenta de manera masiva (más de 10 litros de linfa por día), es una condición que amenaza la vida y es de difícil control, independientemente del tipo de estrategia curativa o paliativa implementada. Hasta el momento no se cuenta con un tratamiento específico para su cura. El arsenal terapéutico más utilizado incluye: suspender la vía oral con nutrición parenteral total, embolización selectiva de vasos linfáticos, ligadura selectiva de vasos linfáticos, infusión lipídica venosa e infusión lipídica linfática, entre otros procedimientos no invasivos que tienen poca efectividad para el tratamiento.
La derivación linfático-venosa múltiple se ha propuesto para el tratamiento de linfedema en extremidades, teniendo como principio fisiológico la reducción de linfa circulando por el sistema linfático, produciendo un shunt que deriva la linfa a la circulación venosa. Se propone en esta revisión, el tratamiento de la quiloascitis masiva que amenaza la vida, con derivaciones linfático-venosas múltiples de manera distal, teniendo como base la reducción de linfa desde la periferia hacia la cavidad abdominal, con reducción total del volumen en fuga a la cavidad abdominal, utilizando de manera innovadora tecnologías para la planeación (linfo-resonancia y ecografía de vasos linfáticos), y la ejecución intraoperatoria de anastomosis microquirúrgica con azul de metileno.
Abstract
Quiloascitis is the excessive accumulation of lymph in the abdominal cavity compared to normal production, which has multiple consequences. Its etiology is diverse, with trauma being the main cause, and in this group are included those secondary to different intra-abdominal surgical procedures, especially those involving manipulation of the retroperitoneum. When it occurs massively (more than 10 liters of lymph per day), it is a life-threatening condition that is difficult to control, regardless of the type of curative or palliative strategy implemented. Until now, there is no specific treatment for its cure. The most commonly used therapeutic arsenal includes: suspending the oral route with total parenteral nutrition, selective embolization of lymphatic vessels, selective ligation of lymphatic vessels, intravenous lipid infusion, and lymphatic lipid infusion, among other non-invasive procedures, which have little effectiveness for treatment.
Multiple venous-lymphatic diversion has been proposed for the treatment of lymphedema in the extremities, with the physiological principle of reducing lymph circulating through the lymphatic system, producing a shunt that diverts the lymph to the venous circulation. The treatment of massive life-threatening quiloascitis is proposed in this review, with multiple distal lymphatic-venous shunts, based on the reduction of lymph from the periphery to the abdominal cavity, with a total reduction of the volume leaking into the abdominal cavity, using innovative technologies for planning (lymphatic resonance and ultrasound of lymphatic vessels), and intraoperative execution of microsurgical anastomosis with methylene blue.
Introducción
La quiloascitis es la acumulación excesiva de linfa en la cavidad abdominal con respecto a la producción normal, que tiene múltiples consecuencias, derivadas desde el punto de vista hemodinámico a la pérdida masiva de líquidos, produciendo una hipovolemia secundaria que, sumada a la alta producción del líquido extravasado del sistema linfático rico en triglicéridos, presenta una alteración de la nutrición, empeorada con la compresión mecánica de la cavidad que contiene todas las vísceras intraabdominales¹⁻³. Su incidencia real es desconocida; no obstante, hay reportes de una incidencia de 1:20.000 a 1:187.000 en Estados Unidos⁴, considerando que los reportes muestran un aumento en el número de casos secundario al aumento en las cirugías retroperitoneales, así como el incremento en la expectativa de vida después de las mismas⁵.
Lo más llamativo de esta enfermedad es la tasa de mortalidad, que oscila entre el 40% y el 70%, con reportes que describen que puede ascender al 90% cuando la quiloascitis es la manifestación de alguna neoplasia⁶⁻⁸, porque también puede presentarse como una malignidad, anormalidades congénitas, obstructivas, inflamatorias, entre otras⁵, ⁶, ⁹.
El diagnóstico de la quiloascitis requiere no solo de la sospecha clínica y observarse en imágenes diagnósticas como la ecografía o la tomografía, sino que requiere confirmación con el líquido obtenido mediante una paracentesis abdominal, que usualmente es de aspecto blanquecino, con un contenido de triglicéridos superior a 200 mg/dl, con celularidad de predominio linfocitario no mayor a 1.200 células por microlitro, con baja concentración de glucosa y de proteínas, con ausencia de microorganismos en su cultivo³, ¹⁰.
Cuando se presenta de manera masiva (más de 10 litros de linfa por día), es una condición que amenaza la vida y es de difícil control, independientemente del tipo de estrategia curativa o paliativa implementada.
Hasta el momento no se cuenta con un tratamiento específico para su cura, teniendo dentro del arsenal terapéutico más utilizado: suspender la vía oral con nutrición parenteral total, octreotide, somatostatina, orlistat, embolización selectiva de vasos linfáticos, ligadura selectiva de vasos linfáticos, infusión lipídica venosa e infusión lipídica linfática, entre otros procedimientos no invasivos que tienen poca efectividad para el tratamiento¹, ⁹.
La derivación linfático-venosa múltiple se ha propuesto para el tratamiento de linfedema en extremidades, teniendo como principio fisiológico la reducción de linfa circulando por el sistema linfático, produciendo un shunt que deriva la linfa a la circulación venosa. Se propone en esta revisión, el tratamiento de la quiloascitis masiva que amenaza la vida, con derivaciones linfático-venosas múltiples de manera distal, teniendo como base la reducción de linfa desde la periferia hacia la cavidad abdominal, con reducción total del volumen en fuga a la cavidad abdominal, utilizando de manera innovadora tecnologías para la planeación (linfo-resonancia y ecografía de vasos linfáticos), y la ejecución intraoperatoria de anastomosis microquirúrgica con azul de metileno.
Reporte de caso
Mujer de 36 años, con antecedente de Lupus eritematoso sistémico (LES) y Síndrome de Sjögren, quien consultó por un mes de dolor inespecífico en fosa ilíaca derecha, asociado a dolor en las articulaciones, pérdida de peso y fiebre. Se le realizó una tomografía axial computarizada (TAC) de abdomen que reportó múltiples adenopatías retroperitoneales derechas, esplenomegalia, adenomegalias mediastinales múltiples y signos inflamatorios ureterales y vesicales. Ante la sospecha de un síndrome linfoproliferativo vs. Infección, decidieron realizar una biopsia de ganglios retroperitoneales vía laparoscópica. Los resultados de la patología reportaron hiperplasia folicular reactiva y cultivos negativos.
Durante la hospitalización, posterior a la laparoscopia, la paciente presentó dolor abdominal, distensión, signos de irritación peritoneal, edema del abdomen que se extendía a los genitales y al miembro inferior derecho (Foto 1). Se le realizó un nuevo TAC de abdomen, el cual reportó ascitis y derrame pleural derecho, para lo cual se le efectuó paracentesis e inserción de dren tipo pigtail (Foto 2), con cultivos infecciosos del líquido negativos hasta la fecha (incluyendo hongos).
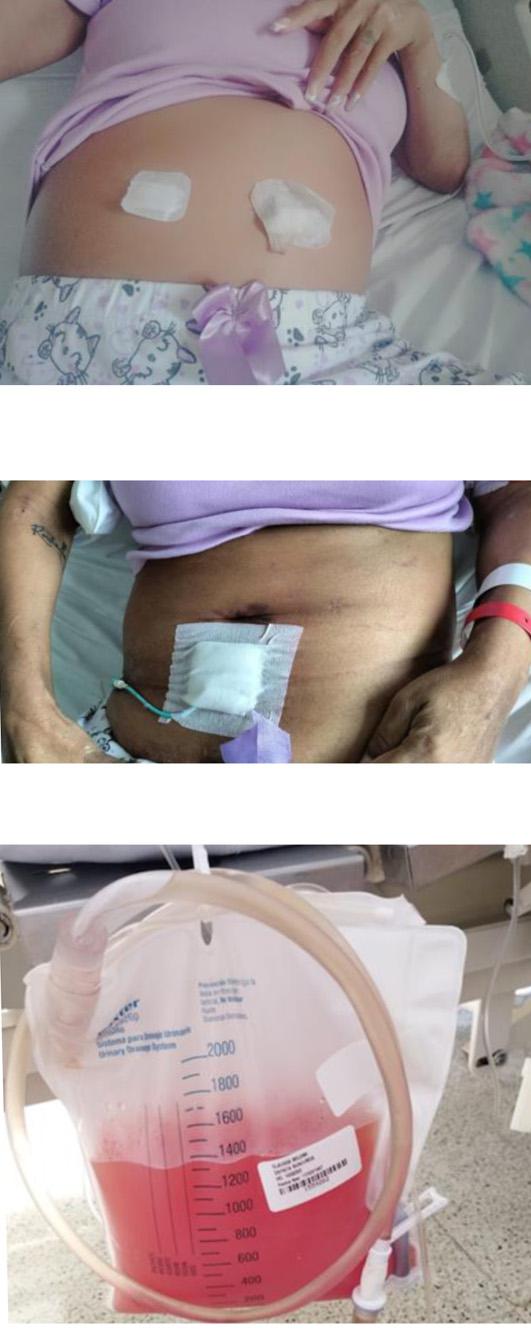
Para el tratamiento, se le inició metilprednisolona en pulsos, como posibilidad de que la ascitis podría explicarse por el LES. Además, se le inició tratamiento con una dieta alta en proteína y baja en grasas, octreotide, somatostatina y orlistat.
Durante los días siguientes se reportó drenaje serohemático muy activo, alrededor de 6.000 cc al día. Se hicieron múltiples análisis del líquido ascítico, los cuales descartaron procesos infecciosos, neoplásicos y reumatológicos.
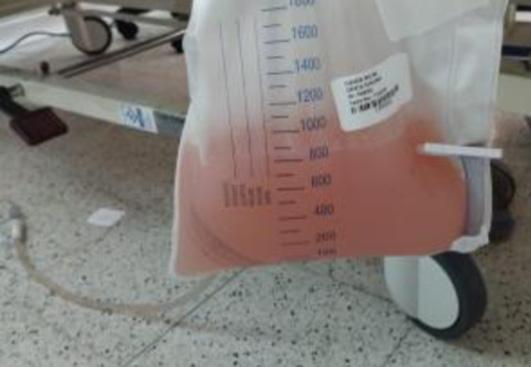
Se obtuvo un aumento marcado del débito por el dren a 11.000 cc por día y las características del líquido ascítico cambiaron de hemático a seroso (Fotos 3-4). Se le realizó una angioresonancia, la cual reportó fístula linfática retroperitoneal (Fotos 5-6). Se decide manejo por linfangiografía con embolización de solución lipídica (lipidol). Luego del procedimiento, el drenaje de líquido ascítico quiloso aumentó, alcanzando valores de hasta 30.000 cc por día. El análisis reportó líquido citrino, 1.250 glóbulos blancos (85% linfocitos), valores de triglicéridos de 1.438 mg/dl, proteínas 2,4 g/dl. Además, la citología, el cultivo y la adenosina deaminasa salieron negativos nuevamente y no hubo cultivos nuevos. Es de resaltar que para este momento la paciente presentó hipoalbuminemia severa (0,8 g/dl).
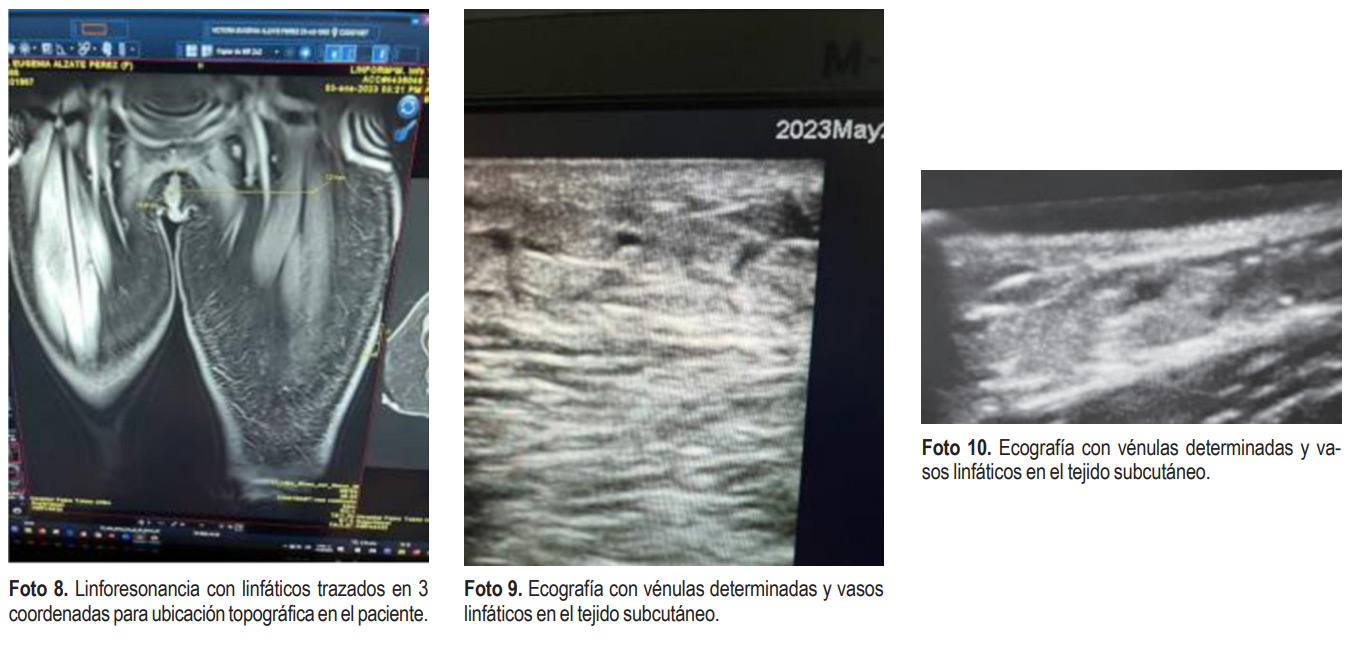
Ante la evolución estacionaria y la confirmación de ascitis quilosa refractaria al tratamiento inicial, se utilizaron las imágenes de linfo-resonancia para determinar el mayor tamaño de los linfáticos (Fotos 7-8) y poder realizar el tratamiento quirúrgico para recanalizar el sistema linfático al sistema venoso, buscando disminuir la carga linfática y drenar al sistema venoso. Se ubicaron las venas de manera prequirúrgica cuando la paciente se encontraba bajo anestesia general con ultrasonido convencional con pieza de mano de 18 megahertz (foto 9-10).
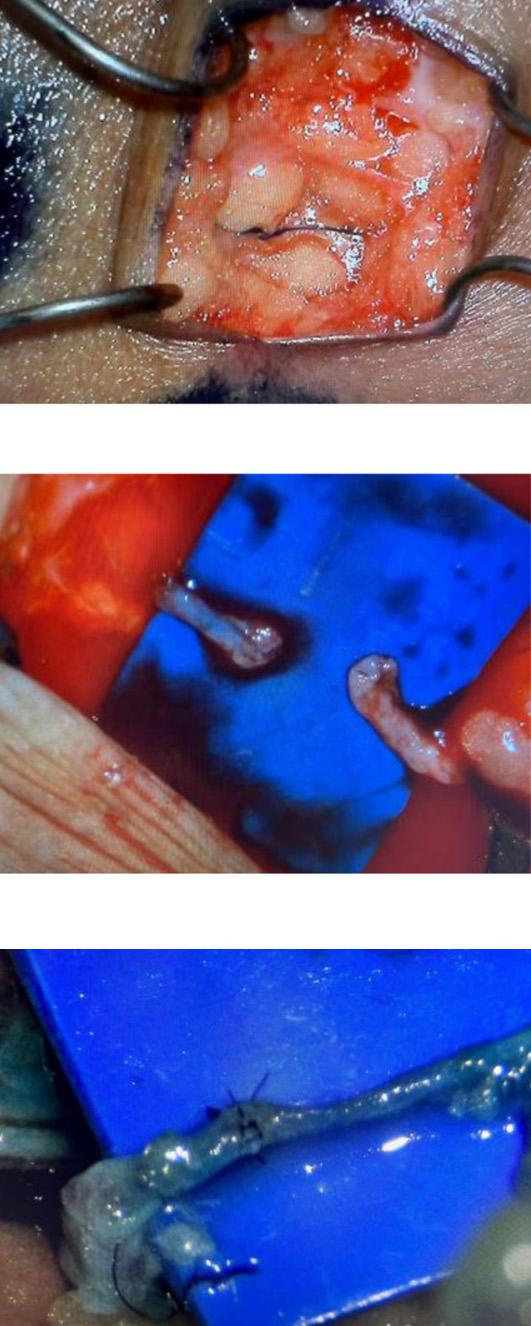
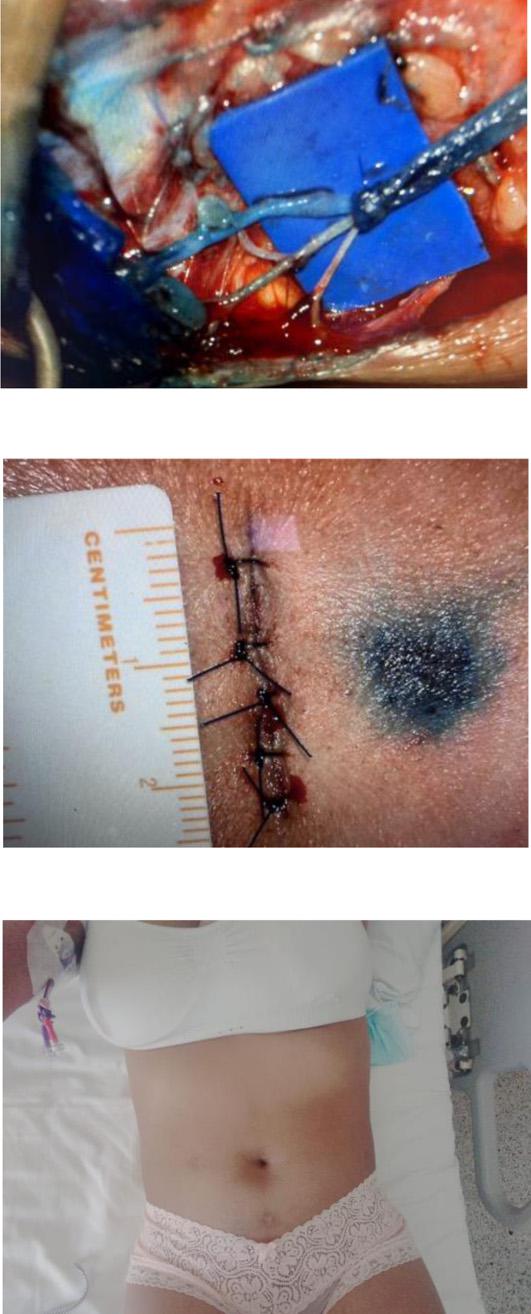
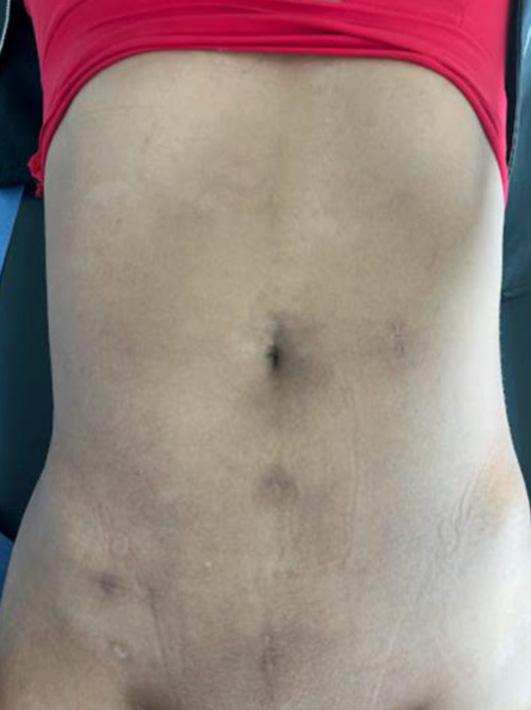
Se efectuó la derivación linfático-venosa múltiple proximal y distal. Se realiza anastomosis linfático-venosa múltiple con un total de 9 derivaciones (Fotos 11-14), con utilización de super microcirugía, mediante incisiones en piel de 2 a 3 cm de longitud, con una visualización previa en linfo-resonancia y ecografía de vasos linfáticos, con un promedio del tamaño de los linfáticos de 0,1 mm a 0,4 mm y con vénulas de 0,3 mm a 0,6 mm. Además de confirmación intraoperatoria de linfáticos con azul de metileno (Foto 15). A las 18 horas del procedimiento, el débito de la quiloascitis bajó a 18.000 cc al día, llegando a la producción de 1.500 cc al día para el sexto día posquirúrgico. Diez días después de la cirugía se retiró el dren (Foto 13) y posteriormente se le dio egreso hospitalario a la paciente. En la consulta de seguimiento de 1 mes posoperatorio se encontró un abdomen sin ascitis, sin salida de secreción por heridas, blando y depresible. Finalmente, en el seguimiento de un año, la paciente sigue sin ascitis y sin síntomas abdominales (Fotos 14-21).

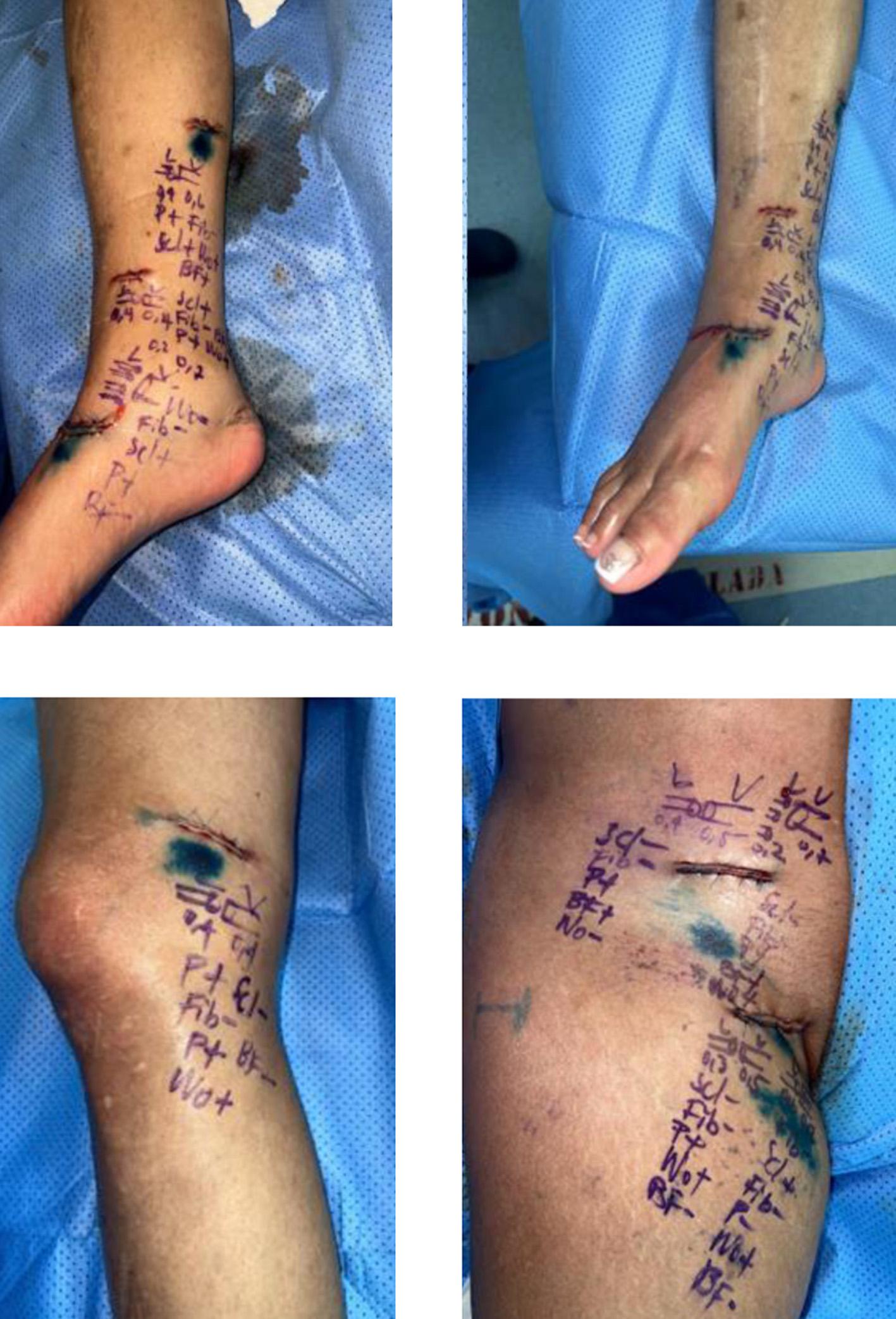
La ascitis quilosa es una entidad caracterizada por la acumulación de quilo en la cavidad abdominal, particularmente rico en triglicéridos, el cual viaja desde el intestino, pasando por vasos linfáticos a la cisterna del quilo y luego por medio del conducto torácico a desembocar al sistema venoso en gran medida en el confluente venoso yugulosubclavio izquierdo. La fisiopatología aún es poco conocida, sin embargo, se sabe que entre los factores implicados están el aumento en la producción del quilo, la obstrucción al drenaje linfático abdominal y alguna forma de traumatismo que produzca injuria en cualquier nivel del sistema linfático. De esta forma, en el contexto quirúrgico podría ser causado por una complicación de cirugías abdominales o retroperitoneales, incluso por complicaciones en biopsia de ganglios linfáticos, como es el caso de la paciente presentada¹'²'⁹.
El tratamiento médico de esta enfermedad es fácil y rápido de instaurar, encaminado a reducir la producción y acumulación del quilo, como lo son una dieta baja en grasas, nutrición parenteral total, octreotide e incluso la paracentesis terapéutica, pero desafortunadamente no cuenta con una alta efectividad, además de que muchos de dichos medicamentos son de alto costo, lo que para una quiloascitis masiva puede resultar en un desenlace fatal³'⁵'¹⁰.
Por eso, después de realizar esta revisión de la literatura disponible hasta la fecha, se concluye que no se cuenta con muchas opciones diferentes a las anteriormente descritas, por eso se propone que las derivaciones linfáticas venosas con la utilización de super microcirugía, sea considerado dentro del arsenal terapéutico dentro de la primera línea, ya que no se reportaron complicaciones en este caso, no genera morbilidad la cirugía, incluso en casos seleccionados se puede realizar bajo anestesia local o espinal, con el fin de lograr una disminución del volumen circulante de linfa dentro del sistema, utilizando drenaje hacia el sistema venoso. Pese a que se considera que el tamaño de los linfáticos de 0,1 o 0,3 mm, no es suficiente para el drenaje, se sabe hoy que el volumen de linfa que circula por ellos es suficientemente grande para descongestionar una extremidad. Además que con la tecnología disponible obtenida en el caso de la paciente, se utiliza la linfo-resonancia y la ecografía, logrando encontrar con mayor precisión los linfáticos y las vénulas susceptibles de anastomosis, corroborando su funcionamiento con azul de metileno y sin tener complicación ni efecto adverso con ninguno de ellos¹'⁹'¹¹'¹²⁻³⁰.
Conclusión
La quiloascitis es una enfermedad rara, usualmente secundaria a la realización de un procedimiento que implica la disección del retroperitoneo, que cuando se presenta de manera masiva, tiene una alta tasa de mortalidad y poca efectividad del tratamiento no quirúrgico. Por lo que se propone, basados en esta revisión de tema y en el caso expuesto de la paciente, que la derivación linfático-venosa con super microcirugía puede ser considerada dentro de las primeras líneas de tratamiento, basados en la efectividad y seguridad del procedimiento.
References
1. Arakaki Y, Shimoji Y, Yamazaki S, Shimizu Y, Aoki Y. Microsurgical lymphaticovenular anastomosis for refractory chylous ascites following para-aortic lymph nodes dissection in a patient with tubal cancer. Gynecol Oncol Rep. 2018 Oct 1;26:53-55.
2. Thiel FC, Parvanta P, Hein A, Mehlhorn G, Lux MP, Renner SP, Preisner A, Beckmann MW, Schrauder MG. Chylous ascites after lymphadenectomy for gynecological malignancies. J Surg Oncol. 2016 Oct;114(5):613-618.
3. Cárdenas A, Chopra S. Chylous ascites. Am J Gastroenterol. 2002 Aug;97(8):1896-900.
4. Steinemann DC, Dindo D, Clavien PA, Nocito A. Atraumatic Chylous Ascites: Systematic Review on Symptoms and Causes. J Am Coll Surg. 2011;212:899- 905.
5. Aalami OO, Allen DB, Organ CH Jr. Chylous ascites: a collective review. Surgery. 2000 Nov;128(5):761-78.
6. Bhardwaj R, Vaziri H, Gautam A, Ballesteros E, Karimeddini D, Wu GY. Chylous Ascites: A Review of Pathogenesis, Diagnosis and Treatment. J Clin Transl Hepatol. 2018 Mar 28;6(1):105-113.
7. Vasko JS, Tapper RI. The surgical significance of chylous ascites.
Arch Surg. 1967;95:355-368.
8. Press O, Press N, Kaufman S. Evaluation and management of chylous ascites. Ann Intern Med 1982;96:258-64.
9. Leibovitch I, Mor Y, Golomb J, Ramon J. The diagnosis and mana- gement of postoperative chylous ascites. J Urol. 2002 Feb;167(2 Pt 1):449-57.
10. Uribe J, Sepúlveda R, Cruz R, Illanes P, Trucco C, Le Roy C, de Barbieri F, Torres J, Stefanelli M, Riquelme A. Ascitis quilosa post cirugía abdominal: caso clínico y revisión de la literatura. Gastro- enterol. latinoam 2018;29:193-199.
11. Yamamoto T, Narushima M, Yoshimatsu H, Seki Y, Yamamoto N, Oka A, Hara H, Koshima I. Minimally invasive lymphatic supermi- crosurgery (MILS): indocyanine green lymphography-guided simulta- neous multisite lymphaticovenular anastomoses via millimeter skin incisions. Ann Plast Surg. 2014 Jan;72(1):67-70.
12. Masia J, Olivares L, Koshima I, Teo TC, Suominen S, van Landuyt K, et al. Barcelona consensus on supermicrosurgery. J Reconstr Microsurg. 2014 ;30(1):53-8.
13. Mihara M, Hara H, Tange S, Zhou HP, Kawahara M, Shimizu Y, et al. Multisite lymphaticovenular bypass using supermicrosurgery technique for lymphedema management in lower lymphedema ca- ses. Plast Reconstr Surg 2016;138(1):262-72.
14. Koshima I, Nanba Y, Tsutsui T, Takahashi Y, Itoh S, Fujitsu M. Minimal invasive lymphaticovenular anastomosis under local anesthesia for leg lymphedema: is it effective for stage III and IV? Ann Plast Surg. 2004;53(3):261-6.
15. Felmerer G, Sattler T, Lohrmann C, Tobbia D. Treatment of various secondary lymphedemas by microsurgical lymph vessel transplantation. Microsurgery. 2012; 32(3):171-7.
16. Patel KM, Manrique O, Sosin M, Hashmi MA, Poysophon P, Henderson R. Lymphatic mapping and lymphedema surgery in the breast cancer patient. Gland Surg 2015;4(3):244-56.
17. Demirtas Y, Ozturk N, Yapici O, Topalan M. Comparison of primary and secondary lower-extremity lymphedema treated with supermi- crosurgical lymphaticovenous anastomosis and lymphaticovenous implantation. J Reconstr Microsurg. 2010;26(2):137-43.
18. Auba C, Marre D, Rodríguez-Losada G, Hontanilla B. Lymphati- covenular anastomoses for lymphedema treatment: 18 months postoperative outcomes. Microsurgery (2012;32(4):261-8.
19. Campisi C, Bellini C, Campisi C, Accogli S, Bonioli E, Boccardo F. Microsurgery for lymphedema: clinical research and long-term results. Microsurgery. 2010;30(4):256-60.
20. Chang DW. Lymphaticovenular bypass for lymphedema manage- ment in breast cancer patients: a prospective study. Plast Reconstr Surg. 2010;126(3):752-8. 10.
21. Campisi C, Davini D, Bellini C, Taddei G, Villa G, Fulcheri E, et al. Lymphatic microsurgery for the treatment of lymphedema. Micro- surgery. 2006;26(1):65-9.
22. Bas CE, Cwykiel J, Siemionow M. A new supermicrosurgery training model of saphenous artery and great saphenous vein anastomosis for development of advanced microsurgical skills. J Reconstr Microsurg. 2017; 33(6):426-34.
23. Wallmichrath J, Baumeister RG, Deglmann CJ, et al. Technique and proof of patency of microsurgical lympho-lymphonodular anasto- moses: a study in the rat model. Microsurgery. 2009;29:303-309.
24. Forte AJ, Huayllani MT, Sisti A, Boczar D, Ciudad P, Manrique OJ, Buntic RF. Assessment of Lymphovenous Anastomosis Patency: Technical Highlights. Plast Reconstr Surg Glob Open. 2020 Mar 27;8(3):e2718.
25. Mukenge SM, Catena M, Negrini D, et al. Assessment and follow-up of patency after lymphovenous microsurgery for treatment of secondary lymphedema in external male genital organs. Eur Urol. 2011;60:1114-1119.
26. Maegawa J, Yabuki Y, Tomoeda H, et al. Outcomes of lympha- ticovenous side-to-end anastomosis in peripheral lymphedema. J Vasc Surg. 2012;55:753-760.
27. Yap YL, Lim J, Shim TW, et al. Patent blue dye in lymphaticovenular anastomosis. Ann Acad Med Singapore. 2009;38:704-706.
28. Mansouri R, Chicken DW, Keshtgar MR. Allergic reactions to patent blue dye. Surg Oncol. 2006;15:58.
29. Wallmichrath J, Baumeister RG, Deglmann CJ, et al. Technique and proof of patency of microsurgical lympho-lymphonodular anasto- moses: a study in the rat model. Microsurgery. 2009;29:303-309.
30. Granzow JW. Lymphedema surgery: the current state of the art. Clin Exp Metastasis. 2018;35:553-558.


