Colgajos locales de estilo libre para la reconstrucción de grandes defectos de pared abdominal: la evolución de los keystone Flap. Serie de casos - Free-style local flaps for the reconstruction of large abdominal wall defects: The Evolution of the keystone Flap. Case series
Palabras clave:
defectos compuestos de pared abdominal, resconstrucción de pared abdominal, colgajos locorregionales, colgajos en isla, colgajos de microperforantes, colgajos keystonekeystone, full-thickness abdominal wall defects, abdominal wall reconstruction, locoregional flaps, island flaps, Microperforator flaps, keystone flapsResumen
La pared abdominal es una estructura miofascial con una extensa cobertura cutánea, cuya función principal es contener y proteger los órganos intraabdominales1. Adicionalmente, contribuye a la movilidad del tronco, estabiliza la columna vertebral, genera aumento en la presión intraabdominal e intratorácica, necesaria para fun- ciones vitales como defecar, toser, vomitar y estornudar, y bajo ciertas circunstancias asiste en la respiración. La pérdida de continuidad, impactará directamente sobre estas funciones generando elevada morbilidad2. Tradicionalmente, los colgajos locales han sido la elección principal para defectos de pequeño a mediano tamaño debido a su simplicidad técnica y baja morbilidad donante1,3. Sin embargo, para defectos extensos, han predominado los colgajos pediculados o libres de otras regiones anatómicas como el muslo y el dorso, a pesar de sus implicaciones en términos de morbilidad adicional y complejidad quirúrgica1,4.
Los colgajos fasciocutáneos en isla tipo keystone, basados en multiperforantes, han emergido como una alternativa prometedora. Esta técnica ha demostrado ser versátil y efectiva en la cobertura de defectos cutáneos de varios tamaños en diversas áreas del cuerpo, destacándose por su bajo riesgo de complicaciones, tiempos quirúrgicos reducidos y resultados estéticos superiores. A pesar de sus ventajas bien documentadas, su aplica- ción específica en la reconstrucción de grandes defectos abdominales ha sido limitada5-10.
El grupo de Cirugía Plástica de la Universidad Nacional de Colombia (PLASTICUN), ha desarrollado modificaciones a la técnica original del colgajo keystone, descrita por Felix Behan en 20036. A esta variante se le ha acuñado el nombre de “colgajos de microperfo- rantes neurovasculares ubicuas locorregionales de lo- calización aleatoria” (UNAL). Las modificaciones introducidas en los colgajos UNAL, incluyen diseccio- nes subfasciales amplias, áreas pediculares pequeñas y diseños de estilo libre adaptativos, que han permitido extender su utilidad hacia defectos de cobertura de moderado a gran tamaño en la región abdominal6,11. Este artículo describe una serie de casos pionera en la literatura médica, analizando las características sociodemográficas, clínicas y los resultados obtenidos con el uso de colgajos UNAL para la reconstrucción de la pared abdominal. Estos hallazgos permiten proponer un nuevo enfoque para el manejo de defectos abdominales en la práctica quirúrgica.
Materiales y métodos
Se presenta un estudio retrospectivo tipo serie de casos. La recolección de datos se llevó a cabo con la aprobación del Comité de Ética del Hospital Universitario Nacional de Colombia. Se realizó un muestreo por conveniencia, identificando los pacientes sometidos a reconstrucción de la pared abdominal entre 2013 y 2024, quienes cumplieron con los siguientes criterios de inclusión: tener 18 años o más, presentar defectos de cobertura de la pared abdominal y haber sido sometidos a reconstrucción quirúrgica con colgajos locorregionales fasciocutáneos en isla, tipo UNAL. Se excluyeron pacientes cuya historia clínica o registros audiovisuales no proporcionaban información completa sobre las variables del estudio.
Todas las cirugías fueron realizadas por dos de los autores. Los procedimientos quirúrgicos incluyeron diseños exclusivamente en isla, estrictamente fascio- cutáneos. Las variables estudiadas se clasificaron en sociodemográficas, clínicas y de desenlace, detalladas en una tabla operativa específica (Tabla 1). Las variables sociodemográficas incluyeron edad, sexo, escolaridad, procedencia y tipo de afiliación al sistema de salud. Las variables clínicas abarcaron la etiología del defecto abdominal, comorbilidades, hábito de tabaquismo, las características del defecto de cobertura y de los colgajos (Tabla 2). Las variables de desenlace contemplaron la estancia hospitalaria, morbilidad en el área donante, la supervivencia del colgajo y las complicaciones posoperatorias (Tabla 3). Las complicaciones fueron subclasificadas en mayores y menores, con el único criterio de haber requerido o no una segunda intervención quirúrgica tras necrosis o dehiscencia extensa que requiriese de otra técnica reconstructiva o no fuesen susceptibles de manejo conservador para propiciar el cierre por segunda intención.
Los datos fueron registrados en una base de datos segura, utilizando la plataforma RedCap, asegurando la confidencialidad y la integridad de la información.
Tabla 1. Variables clínicas.
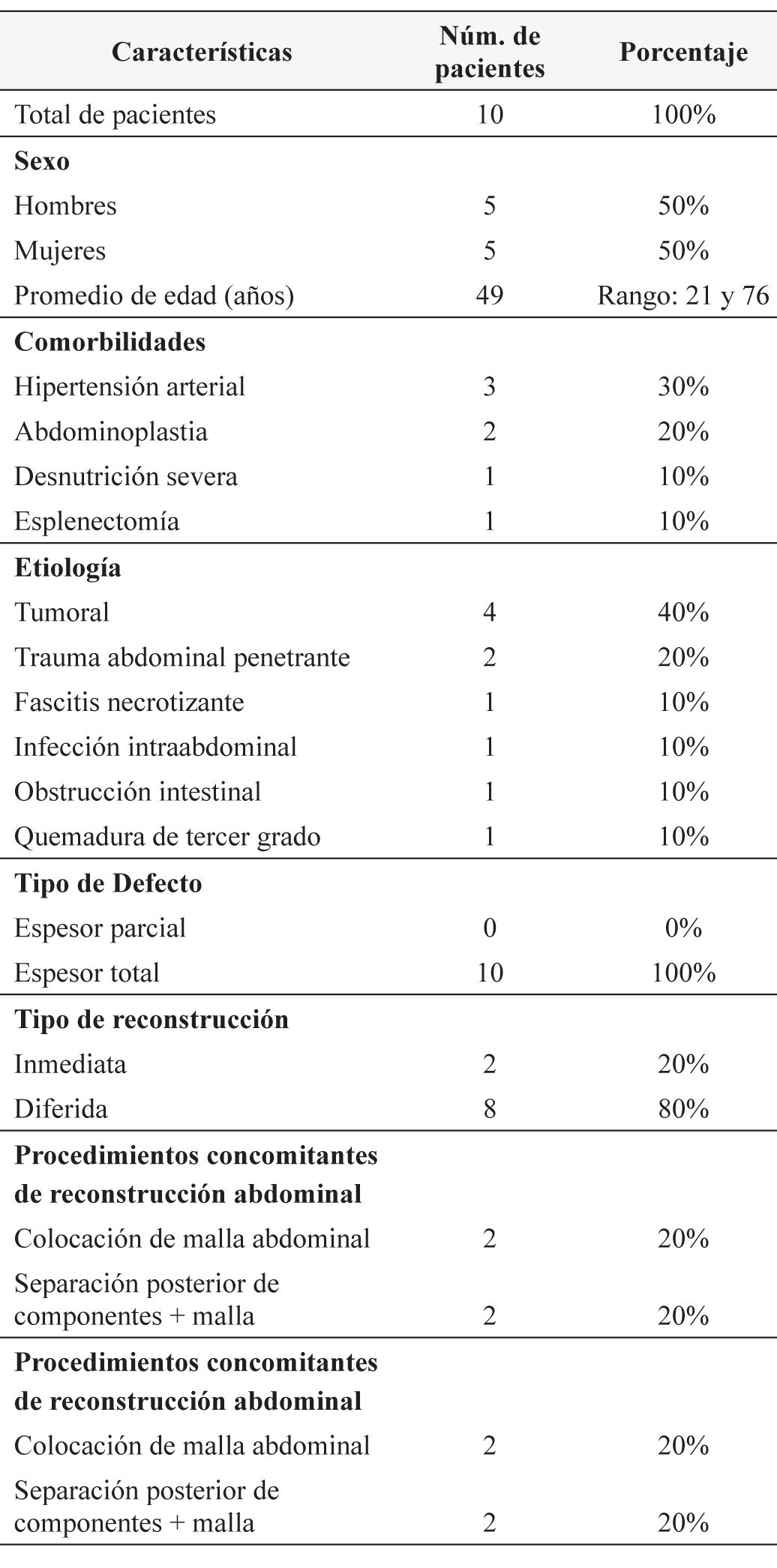
Tabla 2. Características del procedimiento quirúrgico.

Para garantizar la calidad de los datos, dos investigadores revisaron de manera independiente cada historia clínica, resolviendo discrepancias bajo la supervisión del cirujano tratante.
Se obtuvo un consentimiento informado de los participantes, aprobando la publicación del material audiovisual y la información del caso clínico. El análisis de los datos recolectados se realizó utilizando el software STATA 17, proporcionando descripciones detalladas de las variables categóricas y continuas según su distribución.
Técnica quirúrgica
Todas las reconstrucciones se realizaron bajo anestesia general. En los casos de reconstrucciones inmediatas, la cobertura se efectuaba en el mismo tiempo anestésico en el que se generó el defecto abdominal. Así mismo, para los casos que incluían reconstrucción del componente miofascial abdominal, se realizaba en primera instancia la reparación miofascial por parte de los cirujanos de pared abdominal y posterior a ello, en un mismo tiempo quirúrgico, se procedía con la cobertura del defecto cutáneo.
Tabla 3. Desenlaces posoperatorios.

Para las reconstrucciones diferidas, se preparó el lecho quirúrgico mediante procedimientos intermedios como lavados y desbridamientos, asociados al uso de sistemas de presión negativa o de bolsas de laparostomía (Figura 1).
El procedimiento inició con la identificación y caracterización del defecto abdominal y la evaluación de los tejidos perilesionales en términos de laxitud y movilidad. Se documentaron las dimensiones y ubicación de cada defecto. Se diseñaron colgajos exclusivamente en isla sobre la piel abdominal adyacente al defecto. El tamaño y forma de cada colgajo varió de acuerdo con la forma del defecto y su localización, procurando ubicar el eje mayor del colgajo paralelo al defecto. Aunque el área pedicular es cambiante a medida que la disección avanza, usualmente es distal al margen del colgajo adyacente al defecto y en lo posible debe incluir alguno de los pun- tos calientes de la región abdominal, descritos en estudios anatómicos (Figura 2)12-14.
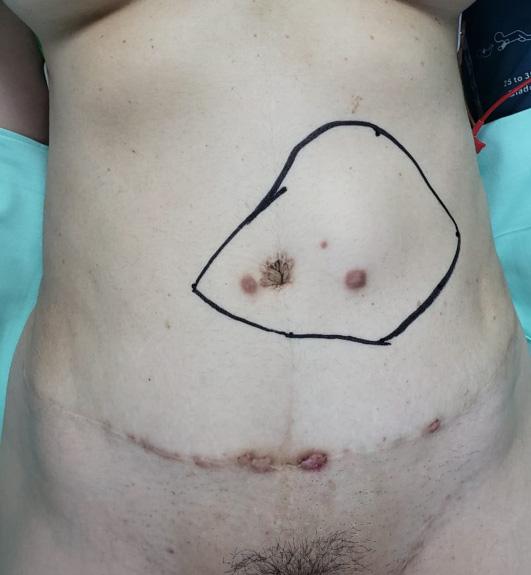
Figura 1. Paciente femenina de 49 años, quien fue llevada a reconstrucción de pared abdominal secundaria a resección de tumor desmoide. Figura 1A. Área de resección tumoral delimitada.
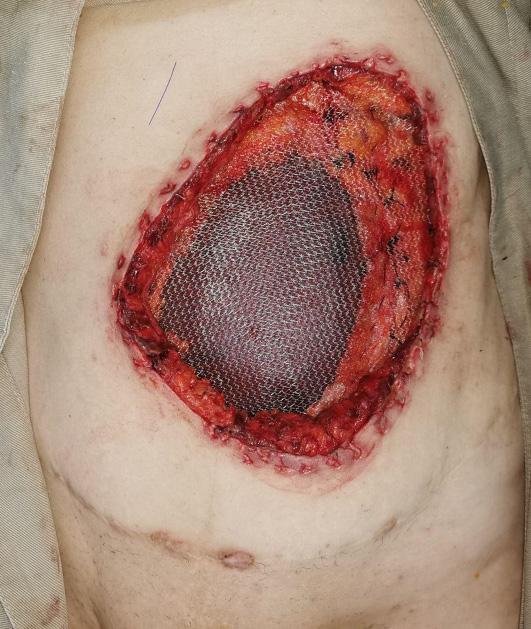
Figura 1B. Defecto de espesor total de 20x10 cm comprometiendo hemiabdomen izquierdo. Se observa malla para reconstrucción de componente miofascial.
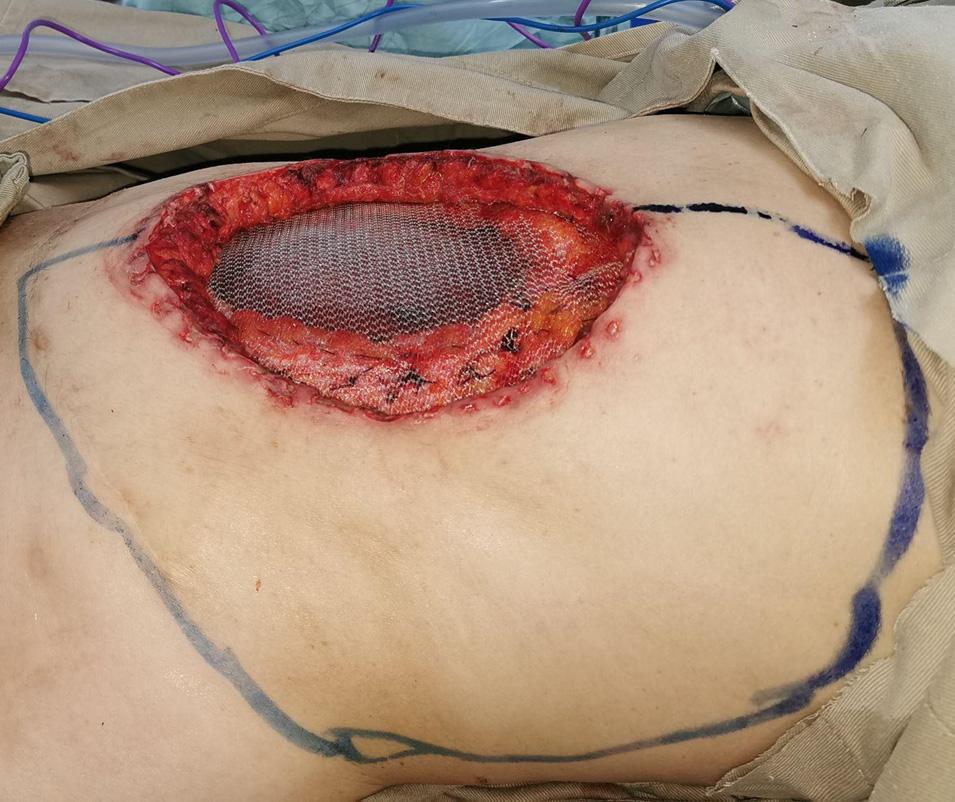
Figura 1C. Diseño de colgajo UNAL de 38x25 cm.
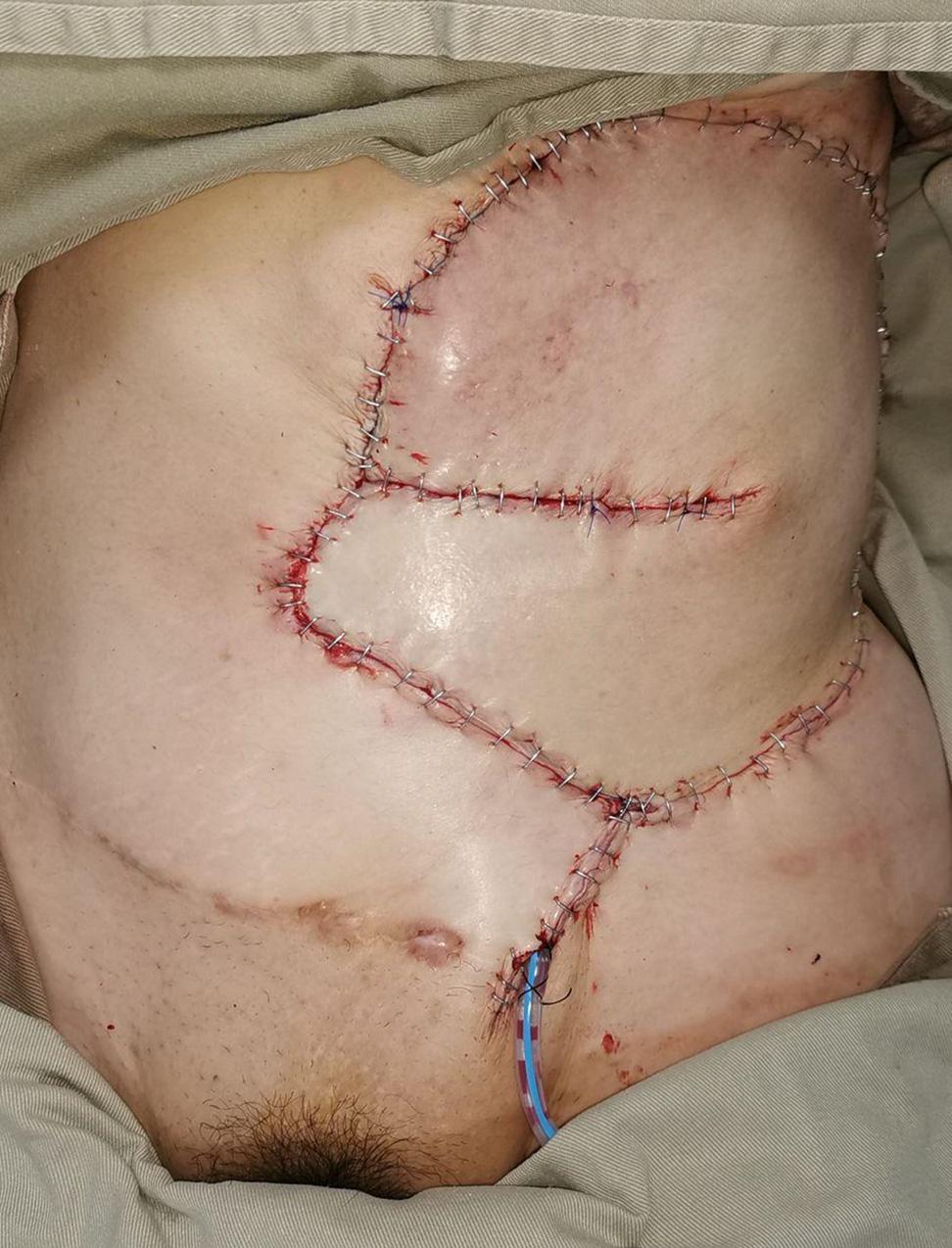
Figura 1D. Posoperatorio inmediato, con cobertura completa del defecto y cierre en omega.
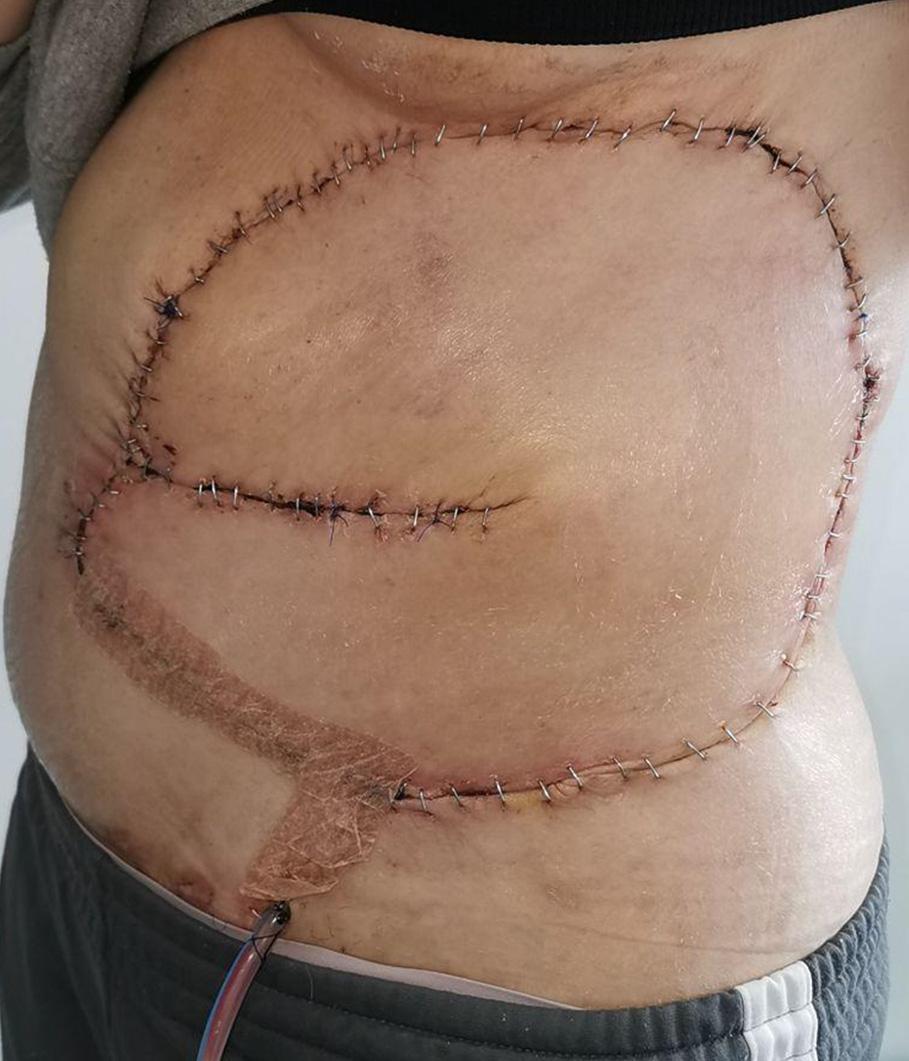
Figura 1E. Día 15 posoperatorio sin complicaciones. Reconstrucción completa y estable del hemiabdomen izquierdo.
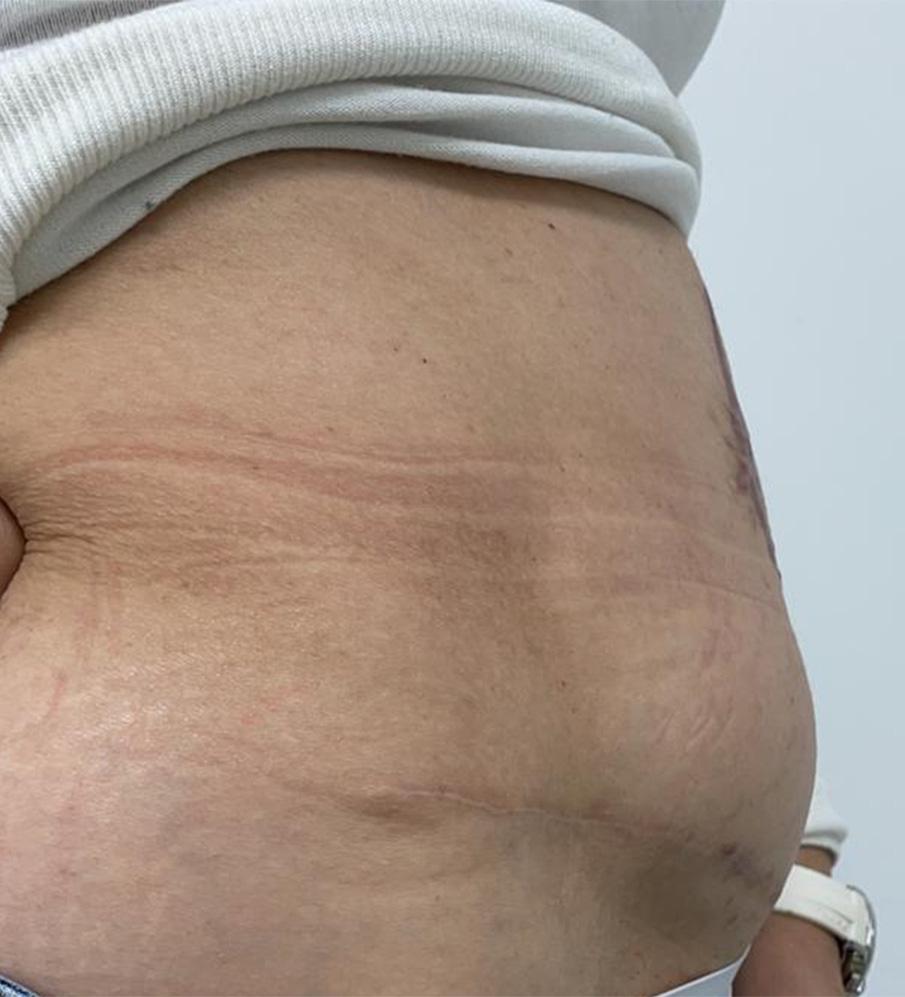
Figura 1F. 3 meses posoperatorio: reconstrucción exitosa, sin herniación, restaurando el contorno abdominal.
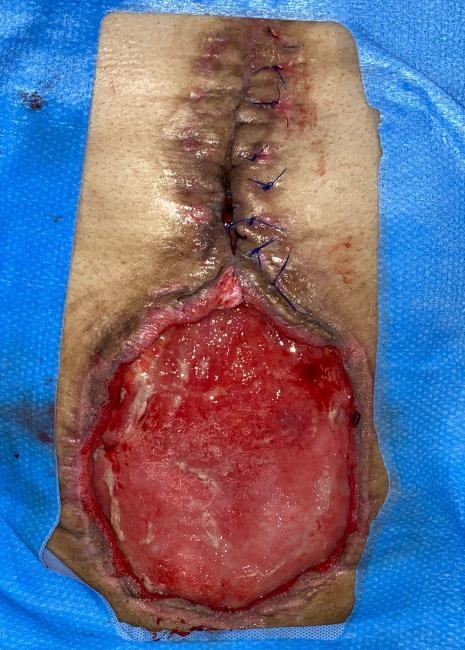
Figura 2. Paciente femenina de 45 años con abdomen en bloque y defecto com- puesto a nivel de línea media, secundario a sepsis abdominal por perforación rectal durante histerectomía. Figura 2A. Defecto de espesor total de 16x15 cm sobre la línea media. Se observa abdomen en bloque.

Figura 2B. Diseño de colgajo UNAL para reconstrucción según subunidades estéticas. Selección de área pedicular del 20% .
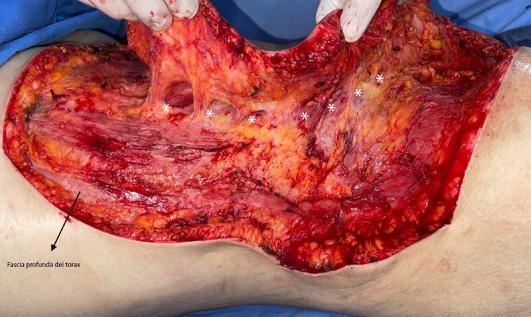
Figura 2C. Disección de colgajo fasciocutáneo en isla de 25x35 cm.

Figura 2D. Área pedicular ubicada sobre la emergencia de los vasos perforantes de las arterias intercostales derecha. No se realiza disección de las mismas ni esqueletonización. (*): perforantes sin disecar.

Figura 2E. Posoperatorio inmediato. Colgajo de avance; permitió reconstrucción de la totalidad de la subunidad estética, restaurando contorno corporal.

Figura 2F. 15 días posoperatorio: sin complicaciones, cobertura estable permite adecuada contención de vísceras abdominales.
Tras el diseño, se incidieron según la marcación to- dos los márgenes de la isla cutánea hasta la fascia. Las disecciones se hicieron subfasciales (a la fascia de scarpa) y la disección procede inicialmente de forma centrípeta, probando con frecuencia el avance logrado a medida que la disección procede. (Cut, see,go, see) hasta lograr la movilización requerida, usualmente de rotación y avance. Se logró la cobertura completa de todos lo defectos. Se dejaron drenes siliconados en el lecho quirúrgico y se realizó un cierre en dos planos; subcutáneo con sutura absorbible multifilamento (vicryl 2/0) y piel con grapas o suturas continuas de monofilamento no absorbible (prolene 3/0, 4/0). Se utilizaron cierres V-Y para algunos extremos cuando se estimó pertinente. Para las áreas donantes se lograron cierres primarios en todos los casos (Figura 3).

Figura 3A. Resección de brida cicatricial en banda comprometiendo tercio superior de abdomen y dorso.
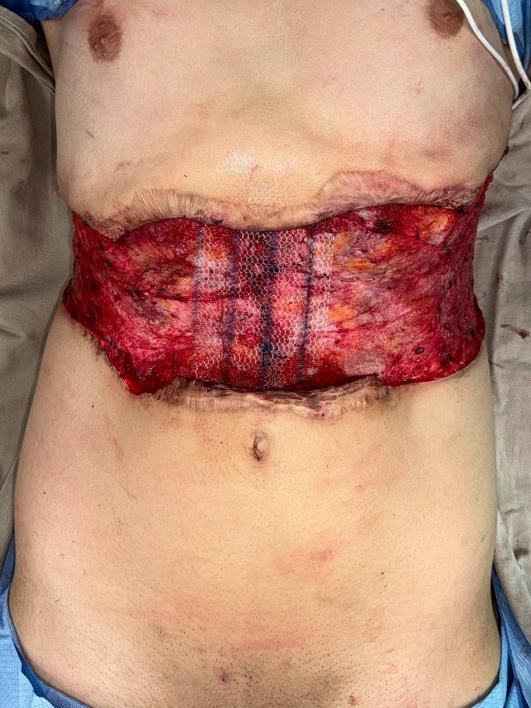
Figura 3B. Reconstrucción miofascial con malla abdominal para corregir eventración secundaria. Defecto de cobertura de 60x15 cm.
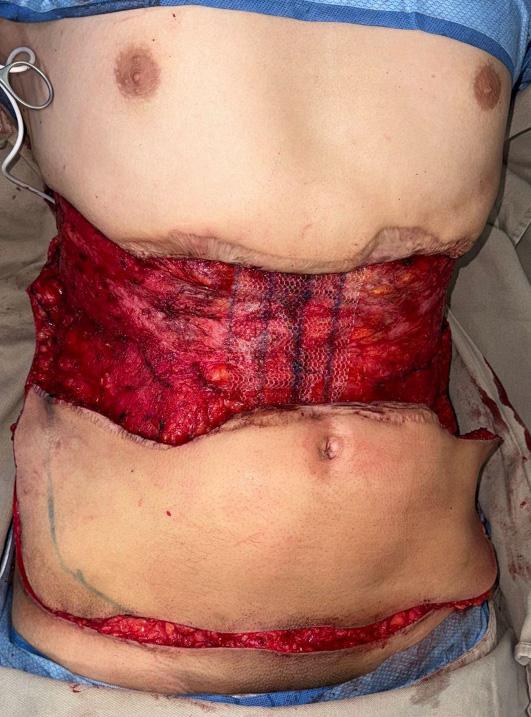
Figura 3C. Colgajo fasciocutáneo en isla tipo UNAL de 35x60 cm, utilizando la totalidad de la pared abdominal anterolateral.
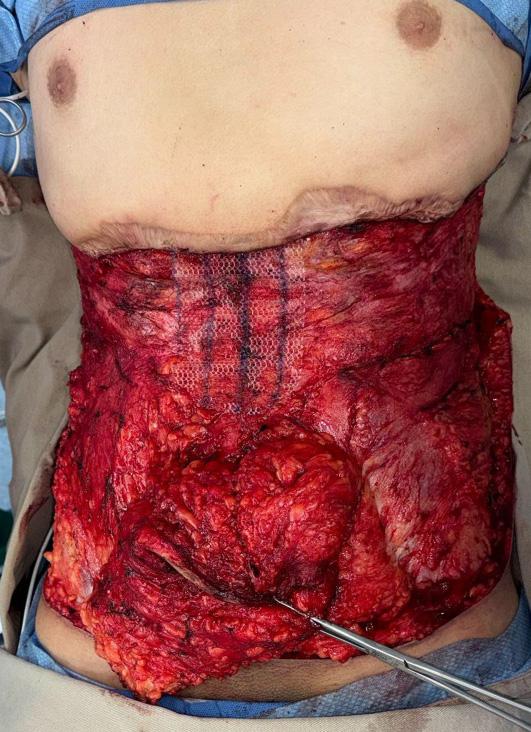
Figura 3D. Disección subfascial centrípeta, desde la periferia hacia el área pedicular. Área pedicular periumbilical del 15%.
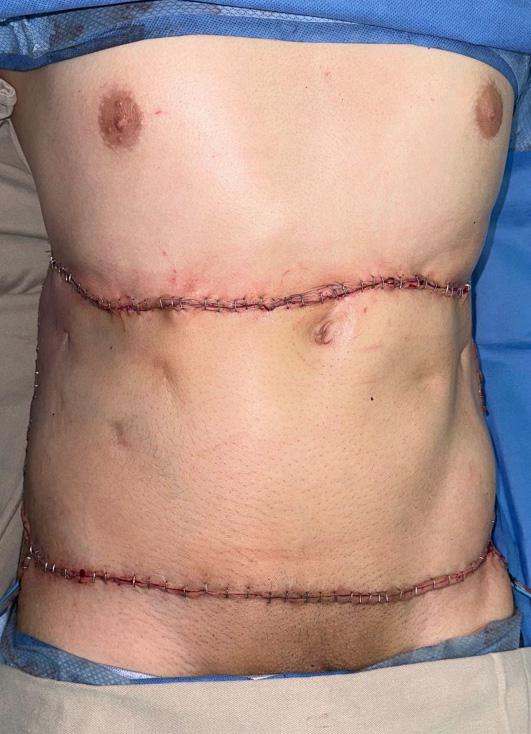
Figura 3E. posoperatorio inmediato, reconstruccion por subunidades exitosa.
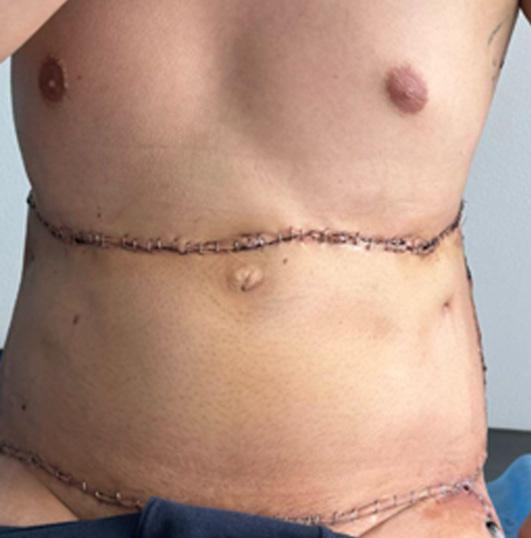
Figura 3F. Dos semanas posoperatorias, colgajo vital, sin complicaciones.
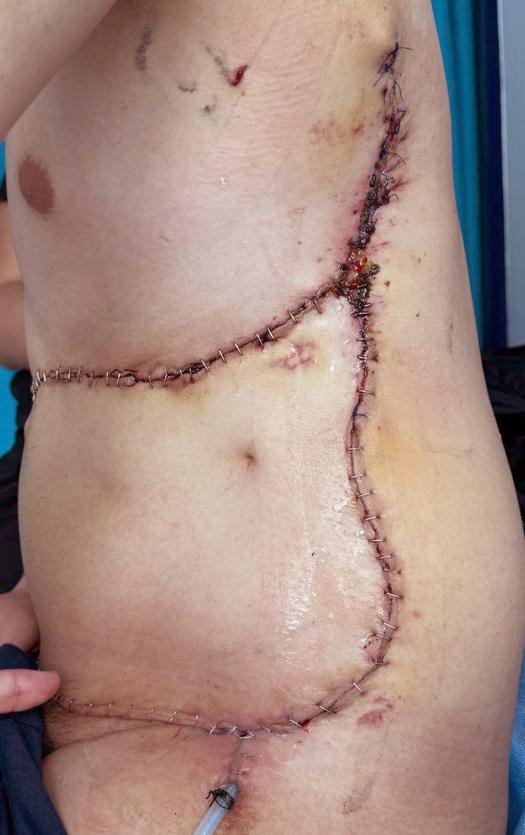
Figura 3G. Reconstrucción exitosa, sin recidiva de herniación.
Al finalizar la cobertura, se evaluó la perfusión del colgajo y de acuerdo a los hallazgos, según la presencia de signos de hipoperfusión, se consideró el uso de toxina botulínica en las áreas hipoperfundidas y alrededor del área pedicular. Esta decisión se dejó a discreción del cirujano.
Resultados
Características sociodemográficas y clínicas
Se incluyeron un total de 10 pacientes con defectos compuestos de la pared abdominal que requirieron reconstrucción quirúrgica con colgajos fasciocutáneos locorregionales en isla tipo UNAL, atendidos entre los años 2013 y 2024. La muestra del estudio abarcó pa- cientes con edades comprendidas entre 21 y 76 años, con una media de 49 años. La proporción entre hom- bres y mujeres fue 1:1. La mayoría de los pacientes pro- cedían del área urbana de la ciudad de Bogotá, Colombia (60%).
Comorbilidades
El 70% de los pacientes presentaban antecedentes médicoquirúrgicos de importancia. El 30% tenía diag- nóstico de hipertensión arterial y hubo dos pacientes con historia de abdominoplastia previa (20%). Un paciente se encontraba en estado de desnutrición debido a hos- pitalización prolongada por sepsis abdominal y otro te- nía antecedente de esplenectomía por trauma abdominal penetrante. Ninguno tenía antecedentes de tabaquismo.
Etiología y procedimientos quirúrgicos
La principal etiología fue la patología tumoral (40%), seguido de trauma abdominal penetrante (20%), fascitis necrotizante (10%), obstrucción intestinal (10%), infección intraabdominal por perforación rectal (10%) y hernia ventral por secuela de quemadura de tercer grado (10%). La mayoría de los defectos de pared abdominal se ubicaron en línea media, esto se observó en el 50% de los pacientes (n=5/10). Los defectos estuvieron distribuidos en: hemiabdomen izquierdo el 30%, tercio su- perior con extensión a región dorsal subescapular el 10%, y el 10% restante en hemiabdomen derecho con extensión a la línea media. Por cuadrantes, el mesogastrio e hipogastrio fueron los sitios más comúnmente compro
metidos por los defectos. Todos los casos presentaron defectos compuestos de la pared abdominal; 5 pacien- tes (50%) tuvieron exposición visceral y 5 (50%) tenían abdomen en bloque.
El 80% de las reconstrucciones fueron diferidas y el 20% inmediatas. El origen del colgajo fue mayoritaria- mente del hemiabdomen derecho (60%), seguido del hemiabdomen izquierdo (30%), y en un caso se utilizó toda la pared abdominal de manera bilateral. El tamaño promedio de los colgajos fue de 771 cm², excluyendo tres colgajos que midieron 32x37 cm (1184 cm²), 35x50 cm (1750 cm²) y 35x60 cm (2100 cm²). El porcentaje de área pedicular utilizada para los colgajos fue princi- palmente de 20-25%. En tres pacientes (30%) se utilizó el 10% o menos. Estas áreas pediculares se basaron en perforantes de distribución aleatoria, provenientes de las vasos intercostales, epigástrica inferior profunda, epigástrica inferior superficial, ilíaca circunfleja superfi- cial y profunda.
El tipo de movimiento realizado por el colgajo fue principalmente rotación y/o avance para cubrir el defec- to de la pared abdominal. En el 40% de los casos se llevaron a cabo procedimientos reconstructivos de pa- red abdominal concomitantes, como la colocación de mallas de refuerzo y la separación posterior de compo- nentes. El tiempo quirúrgico osciló entre 90 y 240 minu- tos, con una media de 162 minutos. En todos los casos, se logró cierre primario del área donante.
Posoperatorio
La supervivencia de los colgajos fue del 100%, com- probada durante todo el periodo de seguimiento. Se presentaron complicaciones mayores en 2 casos. Un paciente cursó con choque hipovolémico asociado a un hemoperitoneo durante el posoperatorio inmediato, requirió drenaje quirúrgico, sin complicaciones. La integridad del colgajo no se vio comprometida. El segundo caso presentó necrosis parcial del 10% de la porción más distal al área pedicular del colgajo. Fue llevado en un segundo tiempo a desbridamiento quirúrgico con cie- rre primario del defecto residual, sin requerir colgajos ni injertos adicionales. Tres pacientes cursaron con com- plicaciones menores. Un paciente cursó con dehiscencia de la herida quirúrgica menor a 2 cm, que fue exitosamente manejada con curaciones. Un paciente presentó una infección profunda del sitio operatorio, la cual fue tratada con antibiótico sistémico por una semana, sin recidivas. Un paciente presentó epidermolisis de 3 cm en cada extremo distal del colgajo, sin necrosis de espe- sor total. Fue tratado con curaciones para cierre por segunda intención, de forma satisfactoria. En cuanto a las complicaciones del área donante, se registraron dos casos de dehiscencia, resueltos con manejo conserva- dor con curaciones locales.
El seguimiento posoperatorio de los pacientes se lle- vó a cabo durante un período de 2 a 31 meses con una media de 15,4 meses. El promedio de estancia hospita- laria fue de 13,1 días (rango: 3-38 días). Tres pacientes presentaron estancias hospitalarias prolongadas de 18 días o más por descompensación de comorbilidades de base, no relacionadas con los colgajos.
Discusión
Los defectos compuestos de la pared abdominal ha- cen referencia a una pérdida de espesor total del com- ponente músculo aponeurótico asociado a defectos de cobertura de los tejidos blandos suprayacentes. Dentro de las etiologías principales se encuentran: 1)Infecciones necrotizantes de tejidos blandos o sepsis de origen abdominal; 2) Trauma; 3) Resección de tumores; 4) Heri- das por radiación o quemaduras, entre otras1,3. Es frecuente que los pacientes con estas patologías cursen con un abdomen abierto, lo cual hace referencia a un defecto abdominal de espesor total, creado quirúrgicamente que permite una exposición visceral controlada con fines terapéuticos. Esta técnica está indicada en cirugías de control de daño secundarias a trauma, manejo de sepsis intraabdominal, hemorragias intraperitoneales, síndrome compartimental abdominal, entre otros. Si bien es una conducta que salva vidas, trae consigo una eleva- da carga en morbimortalidad, debida a una pérdida aumentada de líquidos, electrolitos y proteínas, alteraciones en la mecánica ventilatoria, déficit nutricional con desnutriciones severas y mayor riesgo de infecciones sistémicas, peritonitis, eventraciones y fístulas enteroatmosféricas15,16.
La reconstrucción de la pared abdominal tiene entonces el objetivo de restablecer la continuidad del componente miofascial y proporcionar una cobertura cutánea estable y duradera que permita restaurar la función abdominal, proteger el contenido visceral y minimizar el riesgo de herniación a largo plazo. Teniendo en cuenta el deterioro en la condición de base que presenta la población con defectos abdominales, es imperativo que la reconstrucción proporcione un cierre definitivo, seguro y que no sume a la morbilidad1,3,4,17,18.
De acuerdo con esto, el arsenal de opciones reconstructivas para los defectos abdominales es am- plio, siendo los colgajos de tejidos blandos la principal opción para cobertura cutánea3,4,17. Si bien se ha confir- mado el uso seguro y reproducible de colgajos locales en isla tipo keystone para reconstrucción de grandes defectos en cabeza y cuello, extremidades y tronco pos- terior, su aplicación en cobertura de grandes defectos abdominales (>150 cm2) es escasa19. Esto es debido a que se ha considerado insuficiente la cantidad de tejido local para cubrir defectos de esta magnitud. Adicional mente, para la cobertura de grandes defectos con colgajos locales, se requiere de arcos de movilidad amplios, lo que implica disecciones extensas. Históricamente esto ha sido considerado como potencialmente peligroso al comprometer el aporte vascular3,17. Es por esto que se ha preferido la reconstrucción con colgajos distantes pediculados o libres, principalmente el anterolateral del muslo (ALT) y el dorsal ancho, que si bien ofrecen reconstrucciones estables, aumentan la morbilidad al incidir en otras áreas anatómicas y prolongar los tiempos quirúrgicos3,18,20-23.
Los colgajos de nanoperforantes ubicuas de locali- zación aleatoria (UNAL) nacen a partir de una serie de modificaciones y adaptaciones de los colgajos keystonekeystone descritos por Behan8,10,11. Dentro de sus características destacan:
1. Diseño libre
Modificación del diseño trapezoidal clásico por un diseño de estilo libre que se adapta a las necesidades de cada defecto de forma individual. Esto, sumado al aumento en el tamaño del colgajo, permitió alcanzar una relación defecto: colgajo igual o mayor a 1:3 en esta serie de casos. Esta característica permite la re- construcción por subunidades estéticas, donde los tejidos del colgajo reemplazan completamente la subunidad que contiene el defecto, situando las cicatrices en límites anatómicos, restaurando contornos corporales de forma natural con tejido de características similares, evitando cicatrices disruptivas y mejorando los resultados estéticos, sin necesidad de transgredir otras zonas corporales6,10.
2. Elección del área pedicular basada en puntos calientes
Basado en el concepto fisiológico del angiotoma, entendido este como un segmento tridimensional de piel y tejidos que puede ser elevado como un colgajo en isla y que está vascularizado por un vaso axial, pero que po- dría extenderse a regiones contiguas por sus comunica- ciones con otros vasos axiales adyacentes, mediante los vasos de choque anastomóticos9. La elección del área pedicular, es decir, el área de unión del colgajo a su le- cho por medio de la cual obtiene su vascularización, se hace con base en el conocimiento anatómico de los puntos calientes abdominales6.
La irrigación de la piel y tejido celular subcutáneo de la pared abdominal está dada principalmente por vasos perforantes de las arterias epigástrica superior profunda, epigástrica inferior profunda, epigástrica inferior su- perficial, circunfleja iliaca superficial, circunfleja iliaca profunda e intercostales. Los sistemas epigástricos se anastomosan entre sí en la región periumbilical, y así mismo, presentan anastomosis en la región lateral con los demás sistemas12,24,25. Estudios anatómicos de disecciones cadavéricas humanas han demostrado que los territorios vasculares de estos vasos fuente se sobrelapan entre ellos. Adicionalmente existen áreas anatómicas conocidas donde hay una mayor concentración de va- sos perforantes, tales como la región periumbilical, la zona superior a la cresta iliaca y los septos intermusculares (entre los músculos oblicuos y los rectos). También se han identificado mayor número de anastomosis vasculares entre territorios ipsilaterales que contralaterales12,24,26-28. En los estudios de Hennessy O, Childs C y cols. y Le Saint-Grant A et al., se utilizó la termografía para la identificación y marcación de puntos calientes en la región abdominal. Posteriormente los pacientes fueron llevados a doppler y angiotomografias, donde se evidenció una correlación del 98-97% entre los puntos calientes de la termografía y las áreas anatómicas con mayor presencia de perforantes. Estos hallazgos termográficos coin- cidieron con las disecciones anatómicas previamente descritas13,26,29.
Con base en los conocimientos anatómicos y fisiológicos de la vascularización cutánea, el diseño de los colgajos de microperforantes Ubicuas Neurovasculares Aleatorias (UNAL), fundamenta su aporte vascular en un área aleatoria, donde penetran microperforantes neurovasculares que provienen de las ramificaciones de los vasos perforantes primarios. Estas ramificaciones se interconectan con las ramificaciones de otras perforantes primarias, lo cual permite dar un aporte vascular a todo el territorio cutáneo30. Basar estas áreas de aporte vascular sobre los puntos calientes abdominales previa- mente descritos, hace que no se requiera de la identifi- cación prequirúrgica de las perforantes mediante el uso de doppler u otra ayuda diagnóstica. Tampoco se requiere de la disección y mucho menos la esqueletización del pedículo vascular. Esto tiene un impacto positivo en la reducción de tiempos quirúrgicos, disminuyendo así la dificultad para la reproducción de la técnica. Adicional- mente permite disecciones extensas mayor a dos tercios del área total del colgajo, sin comprometer su perfusión y aumentando el rango de movilidad6.
3. Disecciones en isla y subfasciales
En concordancia con lo descrito por Behan para los colgajos keystone, la disección del colgajo se hace ex- clusivamente en isla, prescindiendo de cualquier puente cutáneo5,8,30. Basado en el concepto de angiosoma y entendiendo la presencia de territorios vasculares diná- micos interconectados por medio de vasos de choque anastomótico, la simpatectomía generada con el trauma quirúrgico al disecar el colgajo en isla, genera una aper- tura de esas anastomosis, redistribuyendo el flujo vascular hacia la periferia del colgajo, sin la necesidad de puentes cutáneos que por el contrario aumentan la resistencia vascular6. Para la presente serie, se llevaron a cabo disecciones amplias cercanas al 90% de la superficie del colgajo, dejando áreas pediculares pequeñas menores al 10%, sin compromiso de la perfusión de los colgajos. Esta variación permite aumentar de manera significativa el rango de movimiento alcanzando rotaciones hasta de 180 grados y por lo tanto haciendo posible el diseño de colgajos en propela.
4. Uso de toxina botulínica a discreción
La toxina botulínica tiene un efecto antagonista del sistema nervioso simpático, bloquea la liberación de norepinefrina, disminuye de forma indirecta la expresión de receptores alfa adrenérgicos en las paredes vasculares e inhibe la liberación de acetilcolina a nivel de la placa neuromuscular, generando parálisis del músculo liso vascular. Es a través de estos mecanismos que la toxina botulínica causa una simpatectomía química, que de igual forma inducirá la vasodilatación de los vasos de choque y redistribuye el flujo en territorios vasculares adyacen- tes. Con base en este mecanismo de acción, la aplicación de toxina botulínica se plantea como una herramienta para optimizar la vascularización de los colgajos en isla, permitiendo ampliar sus tamaños y rangos de movilidad31-34.
Si bien, las ventajas de los colgajos fasciocutáneos en isla tipo keystone han sido ampliamente descritas, estas adaptaciones han permitido expandir su aplicación, haciendo posible la reconstrucción exitosa de defectos de pared abdominal de grandes dimensiones que incluso podrían ser indicación de cobertura con colgajos libres.
Conclusiones
Los defectos de la pared abdominal son una patolo- gía compleja que requiere de una adecuada caracteriza- ción para poder determinar un manejo eficiente. Para el abordaje de defectos de cobertura, se han propuesto varias opciones reconstructivas, que van desde la cica- trización dirigida por segunda intención, los colgajos lo- cales, colgajos pediculados del muslo y el dorso, hasta la cobertura con colgajos libres microvasculares3. A pesar de sus ventajas, el uso de colgajos neurovasculares en isla ha sido limitado para reconstruir defectos de gran magnitud en el abdomen35. Sin embargo, gracias a las modificaciones técnicas planteadas y desarrolladas en los colgajos tipo UNAL, se ha logrado confirmar que este tipo de colgajos son una herramienta reconstructiva muy valiosa y útil para estos escenarios. Ofrecen una técnica sencilla y reproducible con resultados estéticos óptimos, permiten la cobertura completa en un solo tiempo quirúrgico y la realización de procedimientos concomitantes de reconstrucción miofascial. Evitan morbilidad en otras áreas corporales y tienen baja morbilidad del área donante, disminuyendo tiempos quirúrgicos. Todo esto, garantizando una cobertura estable con tejidos bien vascularizados que permiten restaurar la capacidad de protección del contenido abdominal y a su vez reducir costos al sistema de salud.
Referencias
1. Butler CE, Baumann DP, Janis JE, Rosen MJ. Abdominal wall reconstruction. Curr Probl Surg. Dec 2013;50(12):557-86.
2. Flynn W, Vickerton P. Anatomy, Abdomen and Pelvis: Abdominal Wall. In: StatPearls. Trasure Island, Fl; 2023.
3. Baumann DP, Butler CE. Soft Tissue Coverage in Abdominal Wall Reconstruction. Surgical Clinics of North America. Oct 2013;93(5): 1199-209.
4. Althubaiti G, Butler CE. Abdominal Wall and Chest Wall Reconstruction.
Plast Reconstr Surg. May 2014;133(5):688e-701e.
5. Behan F, Sizeland A, Porcedu S, Somia N, Wilson J. keystone island flap: an alternative reconstructive option to free flaps in irradiated tissue. Anz J Surg. May 24, 2006;76(5):407-13.
6. Gómez OJ, Barón OI, Peñarredonda ML. keystone Flap: Overcoming Paradigms. Plast Reconstr Surg Glob Open. Mar 2019;7(3):e2126.
7. Khouri JS, Egeland BM, Daily SD, Harake MS, Kwon S, Neligan PC, et al. The keystone Island Flap: Use in Large Defects of the Trunk and Extremities in Soft-Tissue Reconstruction. Plast Reconstr Surg. Mar 2011;127(3):1212-21.
8. Behan FC. The keystone Design Perforator Island Flap in reconstructive surgery. Anz J Surg. Mar 14 2003;73(3):112-20.
9. Barón Estrada OI. Colgajos tipo keystone: revisión de la literatura.
[Bogotá, Colombia]: Universidad Nacional de Colombia; 2017.
10. Rodríguez-Unda NA, Abraham JT, Saint-Cyr M. keystone and Perforator Flaps in Reconstruction. Clin Plast Surg. Oct 2020;47(4): 635-48.
11. Espinel Pinzón D. Colgajos de nanoperforantes ubicuas de locali- zación aleatoria: serie de casos. [Bogotá D.C]: Universidad Nacio- nal de Colombia; 2023.
12. Rozen WM, Ashton MW, Taylor GI. Reviewing the vascular supply of the anterior abdominal wall: Redefining anatomy for increasingly refined surgery. Clinical Anatomy. Mar 11 2008;21(2):89-98.
13. Childs C, Nwaizu H, Bullivant E, Willmott J, Davies M, Ousey K, et al. Cutaneous Perfusion Dynamics of the Lower Abdomen in Healthy Normal Weight, Overweight and Obese Women: Methods Development Using Infrared Thermography with Applications for Future Wound Management after Caesarean Section. Int J Environ Res Public Health. Mar 14 2023;20(6):5100.
14. Weum S, Mercer JB, de Weerd L. Evaluation of dynamic infrared thermography as an alternative to CT angiography for perforator mapping in breast reconstruction: a clinical study. BMC Med Imaging. Dec 2016 15;16(1):43.
15. Chabot E, Nirula R. Open abdomen critical care management principles: resuscitation, fluid balance, nutrition, and ventilator management. Trau- ma Surg Acute Care Open. Sep 3 2017;2(1):e000063.
16. Centro Provincial de Información de Ciencias Médicas de Granma. A, Vargas Oliva JM, Arias Aliaga A, Vargas Oliva JM. Multimed. [Internet]. Vol. 23, Multimed. Departamento Editorial, Centro Pro- vincial de Información de Ciencias Médicas de Granma; 2019 [cited
2024 Jun 23]. 189-203 p. http://scielo.sld.cu/scielo.php?script=sci_ arttext&pid=S1028-48182019000100189&lng=es&nrm=iso&tlng=es
17. Patel NG, Ratanshi I, Buchel EW. The Best of Abdominal Wall Reconstruction. Plast Reconstr Surg. Jan 2018;141(1):113e-36e.
18. Leppäniemi A, Tukiainen E. Reconstruction of Complex Abdomi- nal Wall Defects. Scandinavian Journal of Surgery. Mar 1 2013; 102(1):14-9.
19. Wanjala NF, Dan K. Local/regional flaps for extensive abdominal wall defects: Case series. Int J Surg Case Rep. 2020;74:10-4.
20. Di Summa Pg, Watfa W, Campisi C, Giordano S, Oranges CM, Elahi- Rausis L, et al. Free Versus Pedicled Anterolateral Thigh Flap for Abdominal Wall Reconstruction. Anticancer Res. Dec 62019;39(12): 6759-68.
21. Hsieh PJ, Shi MY, Pu CM. Subtotal Thigh Flap for Large Abdominal Wall Defect Reconstruction in Patient With Recurrent Dermatofibrosarcoma Protuberans. Ann Plast Surg. Jan 2024;92(1S):S41-4.
22. Kagaya Y, Arikawa M, Higashino T, Miyamoto S. Autologous abdo- minal wall reconstruction using anterolateral thigh and iliotibial tract flap after extensive tumor resection: A case series study of 50 consecutive cases. Journal of Plastic, Reconstructive & Aesthetic Surgery. Apr 2020;73(4):638-50.
23. Wong CH, Lin CH, Fu B, Fang JF. Reconstruction of Complex Abdo- minal Wall Defects with Free Flaps: Indications and Clinical Outcome. Plast Reconstr Surg. Aug 2009;124(2):500-9.
24. Rahn DD, Phelan JN, Roshanravan SM, White AB, Corton MM. Anterior abdominal wall nerve and vessel anatomy: clinical implications for gynecologic surgery. Am J Obstet Gynecol. Mar 2010;202(3):234.e1-234.e5.
25. Bergeron L, Tang M, Morris SF. The Anatomical Basis of the Deep Circumflex Iliac Artery Perforator Flap with Iliac Crest. Plast Reconstr Surg. Jul 2007;120(1):252-8.
26. Le Saint-Grant A, Taylor A, Varsou O, Grant C, Cezayirli E, Bowness
J. Arterial anatomy of the anterior abdominal wall: Ultrasound evaluation as a real-time guide to percutaneous instrumentation. Clinical Anatomy. Jan 8 2021;34(1):5-10.
27. Isaac K V., Buchel EW. Truncal-based perforator flaps for autologous breast reconstruction: A review of 975 flaps and their clinical application. Microsurgery. May 8 2022;42(4):341-51.
28. Khansa I, Janis JE. Management of skin and subcutaneous tissue in complex open abdominal wall reconstruction. Hernia. Apr 4 2018;22(2):293-301.
29. Hennessy O, Potter SM. Use of infrared thermography for the assessment of free flap perforators in autologous breast reconstruction: A systematic review. JPRAS Open. Mar 2020;23:60-70.
30. Behan FC, Rozen WM, Lo CH, Findlay M. The omega -Ω- variant
designs (types A and B) of the keystone perforator island flap. Anz J Surg. Sep 2011;81(9):650-2.
31. Huang L. Beneficial effect of botulinum toxin A on secondary ischaemic injury of skin flaps in rats. British Journal of Oral and Maxillofacial Surgery. Feb 2018;56(2):144-7.
32. Motegi S, Sekiguchi A, Saito S, Ishibuchi H, Kishi C, Yasuda M, et al. Successful treatment of Raynaud’s phenomenon and digital ulcers in systemic sclerosis patients with botulinum toxin B injection: Assessment of peripheral vascular disorder by angiography and dermoscopic image of nail fold capillary. J Dermatol. Mar 22 2018;45(3):349-52.
33. Shen Y, Lee Y, Leong P. Botulinum toxin injection for refractory Raynaud phenomenon and digital ulcers in systemic sclerosis. Int J Rheum Dis. Feb 26 2023;26(2):187-9.
34. Bello RJ, Cooney CM, Melamed E, Follmar K, Yenokyan G, Leatherman G, et al. The Therapeutic Efficacy of Botulinum Toxin in Treating Scleroderma-Associated Raynaud’s Phenomenon: A Randomized, Double-Blind, Placebo-Controlled Clinical Trial. Arthritis & Rheumatology. Aug 26 2017;69(8):1661-9.
35. Seretis K, Bounas N, Lykoudis EG. Reconstruction of midline abdo- minal defects with a deep inferior epigastric artery keystone-type perforator flap. Journal of Plastic, Reconstructive & Aesthetic Surgery. Feb 2022;75(2):893-939.


